АНЕСТА®-А: ВСТРЕЧАЕМ НОВЫЙ ПРЕПАРАТ ДЛЯ ПОВЕРХНОСТНОЙ АНЕСТЕЗИИ
13.10.2020
Терентьева Лада Владимировна
К.м.н., врач-дерматоловенеролог, косметолог.
Доцент кафедры дерматологи-венерологии РНИМУ им. Н.И. Пирогова.
Сертифицированный эксперт Федеральной службы по надзору в сфере здравоохранения при осуществлении государственного контроля и безопасности медицинской деятельности в области дерматовенерологии, косметологии.
Ведущий специалист-косметолог в отделении ФГБУ «Кремлевская больница».
Ведущий специалист и основатель Beauty Class Clinic, Москва
Местная анестезия в эстетической медицине и дерматологии может быть обеспечена несколькими способами. У всех этих методик есть свои достоинства и недостатки, и выбор конкретного способа диктуется особенностями выполняемых манипуляций. Аппликационная, или поверхностная, анестезия заключается в нанесении местного анестетика на кожу или слизистую оболочку. Несмотря на то что для достижения обезболивания необходимо довольно долгое время, для многих процедур этот способ является самым приемлемым вариантом: аппликационная анестезия проста в применении, совершенно нетравматична, комфортна для пациента, сопряжена с незначительными побочными эффектами, пригодна для использования на больших участках обрабатываемой поверхности и более безопасна с точки зрения токсического воздействия, чем, например, инфильтрационная, а постепенное проникновение действующего вещества через кожу обеспечивает необходимый эффект длительностью до нескольких часов.
До недавнего времени в распоряжении косметологов и дерматологов было всего два препарата, официально зарегистрированных в качестве аппликационных анестетиков, — Эмла® (Recipharm Karlskoga AB, Швеция) и Акриол Про (АО «Акрихин», Россия). Учитывая, что приказом Минздрава России от 18.03.2020 № 188 действие регистрационного удостоверения Эмла® было приостановлено, появление еще одного препарата аналогичной направленности и эффективности стало как нельзя более актуальным. Такое средство — крем Анеста®-А (Argumentum Holding AG, Швейцария)* — недавно прошло регистрацию и стало доступным для практикующих специалистов.
(* Производственная площадка: Agio Pharmaceuticals, Ltd., Индия.)
Состав препарата
В качестве активных веществ Анеста®-А содержит амидные анестетики лидокаин и прилокаин в виде эвтектической смеси в соотношении 1 : 1, где содержание каждого из действующих веществ составляет 2,5% (или по 25,0 мг на 1 г крема). Такая смесь плавится при температуре 18 °С, тогда как в отдельности и лидокаин, и прилокаин имеют намного более высокие температуры плавления, так что в составе эмульсии отдельно взятый анестетик может кристаллизоваться, что снижает его эффективность. Эвтектика же при нанесении уже находится в жидком состоянии, что облегчает проникновение через интактные кожные покровы и слизистые оболочки. Низкое содержание анестетиков в креме обусловливает его токсикологическую безопасность; при этом основное количество эвтектической смеси (около 80%) сосредоточено в каплях внутренней фазы эмульсии [1], которые и обеспечивают эффективную доставку в кожу.
В качестве вспомогательных веществ в состав 1 г препарата входят: макрогола глицерилгидроксистеарат 17,0 мг, натрия метилпарагидроксибензоат (натрий метилпарабен) 1,0 г, натрия пропилпарагидроксибензоат (натрий пропилпарабен) 0,1 мг, циклометикон 20,0 мг, карбомер 974 Р 8,0 мг, натрия гидроксид 4,1 мг, вода очищенная до 1 г.
Механизм действия
 Крем, нанесенный на интактную кожу под плотную повязку, обеспечивает местную анестезию за счет проникновения лидокаина и прилокаина в эпидермис и дерму и накопления действующих веществ вблизи болевых рецепторов и нервных окончаний кожи.
Крем, нанесенный на интактную кожу под плотную повязку, обеспечивает местную анестезию за счет проникновения лидокаина и прилокаина в эпидермис и дерму и накопления действующих веществ вблизи болевых рецепторов и нервных окончаний кожи.
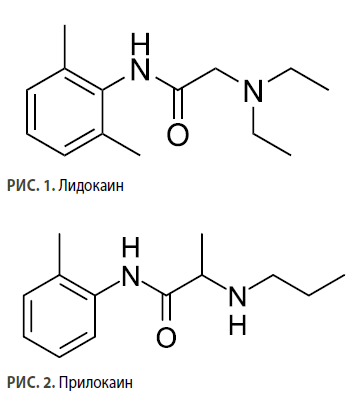
Строение молекул лидокаина и прилокаина типично для амидных анестетиков: в молекуле присутствует бензольное кольцо (липофильная часть) и концевая аминогруппа (третичная в случае лидокаина и вторичная — у прилокаина), связанная с ароматическим циклом через амидную цепь (рис. 1, 2). Липофильная часть молекулы отвечает за проникновение анестетика через периневрий и мембраны нейронов. С этим напрямую связана сила действия препарата. Связывание с тканевыми белками определяет длительность эффекта: чем оно сильнее, тем дольше длится действие средства. Гидрофильная аминогруппа связывается с рецепторами на внутренней поверхности мембраны нервного волокна и отвечает за скорость развития эффекта: чем ближе показатель константы диссоциации к физиологическому рН (7,35–7,45), тем выше концентрация липофильной неионизированной формы действующего вещества, проникающей через мембрану нейрона, и тем быстрее наступает анестезия. Это объясняет, например, тот факт, что при воспалительном процессе с характерным для него более низким рН (5-6) для наступления анестезии требуется больше времени. А вот во внутриклеточном пространстве с рецепторами в натриевых каналах связывается только катионная форма молекулы.
По совокупности свойств лидокаин и прилокаин относятся к быстродействующим анестетикам средней мощности со средней продолжительностью действия, однако совместное их применение обеспечивает синергичное усиление эффекта [2, 3]. В отличие от сложноэфирных анестетиков (новокаин, тетракаин), лидокаин и прилокаин не разрушаются эстеразами и действуют дольше; к тому же амиды практически не вызывают аллергических реакций.
Клиническое исследование эффективности
В 2016 г. было проведено мультицентровое слепое сравнительное рандомизированное плацебо-контролируемое клиническое исследование эффективности и безопасности Анеста®-А в сравнении с кремом Эмла® в качестве местноанестезирующего средства при коррекции мимических морщин в области лба и межбровной зоне. Ввиду явных различий упаковки и маркировки тест- и референс-препаратов и невозможности переупаковывания оригинального препарата двойное слепое исследование провести не представлялось возможным, но разработанный протокол предусматривал «ослепление» участников исследования, рандомизацию и плацебо-контроль относительно обоих препаратов. Состав плацебо-крема полностью соответствовал составу Анеста®-А, за исключением действующих веществ. Для увеличения объективности были проведены предварительное определение болевого порога каждого участника с применением иглы, а также косвенная оценка болевой чувствительности с использованием прибора-гальванизатора для электрофореза типа «Поток» в день рандомизации минимум за 60 мин до нанесения исследуемых препаратов. Средние значения болевого порога у участников обеих групп статистически не различались.
Участники мужского и женского пола в возрасте 24–59 лет, отобранные в ходе скрининга в соответствии с критериями включения, были случайным образом распределены на две параллельные группы по 60 человек: тест-препарат + плацебо и референс-препарат + плацебо. Статистически значимые различия между группами по половому признаку и возрасту не выявлены.
Исследуемые кремы (анестетик и плацебо) в дозировке 1,5–2 г на 10 см2 наносили на интактную очищенную кожу лба участников в местах предполагаемых инъекций на 60 ± 5 мин толстым слоем под окклюзионную повязку. По окончании экспозиции кремы удаляли ватным диском, смоченным 0,05% раствором хлоргексидина, после чего проводили процедуру коррекции морщин в соответствии с методикой применения препарата ботулинического токсина типа А (100 ед/флакон) в дозировках, определенных в зависимости от индивидуальной потребности. При этом различия по общей дозе ботулинического токсина между группами были статистически незначимы. Параллельно проводилась оценка боли по визуально-аналоговой шкале (ВАШ) и оценка удовлетворенности анестезией по 3-балльной шкале. Длительность сохранения местноанестезирующего эффекта оценивали по восстановлению исходной болевой чувствительности с применением иглы через 2 ч после процедуры коррекции морщин.
Статистический анализ данных показал, что и тест-, и референс-препараты были достоверно эффективнее в отношении снижения боли по ВАШ, чем плацебо; при этом различия между Анеста®-А и Эмла® были несущественными. Аналогичные результаты были получены в отношении субъективной оценки удовлетворенности анестезией и времени восстановления болевой чувствительности.
Безопасность исследуемых препаратов оценивали по уровню и характеристике наблюдаемых нежелательных явлений.
Все участники завершили исследование. Нежелательных явлений у участников исследования не отмечено. Оценка показателей безопасности (клинический и биохимический анализ крови, общий анализ мочи, ЭКГ, жизненные показатели) свидетельствовала об отсутствии клинически значимых изменений, связанных с применением исследуемых анестетиков. Переносимость всех препаратов у всех участников оценена как хорошая. Значимых различий по безопасности внутри групп и между группами установлено не было.
Таким образом, данные сравнительного клинического исследования позволяют сделать вполне однозначный вывод о том, что Анеста®-А по эффективности и безопасности не уступает препарату сравнения.
Области применения
Показания к применению Анеста®-А включают следующие случаи [4]:
- поверхностная анестезия кожи при инъекциях (включая вакцинацию), пункциях, катетеризации сосудов, поверхностных хирургических вмешательствах — в том числе и у детей;
- поверхностная анестезия при небольших косметологических процедурах;
- поверхностная анестезия трофических язв нижних конечностей при хирургической обработке (механической очистке);
- поверхностная анестезия слизистой оболочки половых органов при проведении болезненных манипуляций и для обезболивания перед инъекциями анестетиков.
В эстетической медицине и дерматологии крем Анеста®-А может быть рекомендован для обезболивания с целью поверхностной анестезии при [4]:
- инъекциях (мезотерапия, ботулинотерапия, контурная пластика) — при необходимости в сочетании с другими видами анестезии [5, 6];
- различных лазерных процедурах, включая удаление татуировок [7, 8];
- дермабразии [5];
- эпиляции различными методами [5];
- косметическом и перманентном татуаже [5, 9];
- криотерапии (в том числе и на слизистых оболочках половых органов) [10, 11];
- удалении папиллом, бородавок, контагиозного моллюска;
- обезболивании перед инъекциями местных анестетиков.
Способ применения и дозы препарата в косметологии и дерматологии
При проведении косметологических и дерматологических процедур Анеста®-А применяется наружно, методом аппликации на кожу или слизистые оболочки. Рекомендуемые дозировки и режимы применения у взрослых и детей приведены в таблице. Следует отметить, что полоска крема длиной 3,5 см примерно соответствует дозе 1 г.
Таблица. Рекомендации по применению Анеста®-А в дерматологии и косметологии
|
Цель |
Показания |
Доза |
Способ нанесения |
Время воздействия |
|
Анестезия интактной кожи у взрослых |
Перед инъекциями |
Около 2 г на 10 см2 |
Толстым слоем* под окклюзионную повязку |
Не менее 1 и не более 5 ч |
|
Небольшие поверхностные хирургические вмешательства (удаление контагиозного моллюска, бородавок) |
1,5–2 г на 10 см2 |
|||
|
Небольшие косметологические процедуры, эпиляция |
||||
|
Поверхностные хирургические процедуры на больших площадях (в стационаре) |
Не менее 2 и не более 5 ч |
|||
|
На большие площади свежевыбритой кожи (амбулаторно), в том числе перед эпиляцией |
Не более 60,0 г на площадь не более 600 см2 |
Не менее 1 и не более 5 ч |
||
|
Поверхностная анестезия половых органов у взрослых |
На кожу половых органов у женщин перед инъекцией |
1–2 г на 10 см2 |
Толстым слоем*. Окклюзионной повязки не требуется |
60 мин |
|
На кожу половых органов у мужчин перед инъекцией |
1 г на 10 см2 |
15 мин |
||
|
На слизистые оболочки половых органов при удалении кондилом и для обезболивания перед инъекциями местных анестетиков |
5–10 г в зависимости от площади обрабатываемой поверхности |
На всю поверхность слизистой оболочки, включая складки. Окклюзионной повязки не требуется |
5–10 мин; процедуру проводит сразу после удаления крема |
|
|
Поверхностная анестезия кожи у детей |
Перед инъекциями, при удалении контагиозного моллюска и при небольших поверхностных хирургических вмешательствах |
1 г на 10 см2; при этом максимальная обрабатываемая площадь должна составлять не более: 0–3 мес — 10 см2; 3–12 мес — 20 см2; 1–6 лет — 100 см2; 6–12 лет — 200 см2 |
Толстым слоем* под окклюзионную повязку |
0–3 мес — 1 ч, но не более; 3–12 мес — 1 ч; 1–12 лет— не менее 1 и не более 4 ч |
* Кожу не должно быть видно под слоем крема.
Особенности использования
Для обеспечения эффективности Анеста®-А при накожном применении нанесение крема под окклюзионную повязку обязательно, иначе абсорбция действующих веществ заметно снижается из-за быстрого испарения воды и уменьшения содержания влаги в роговом слое.
Имеются данные по влиянию удельного количества наносимого крема лидокаина + прилокаина на эффективность обезболивания у детей [12]: при нанесении тонким слоем (0,5 г/10 см2) некоторые дети ощущали слабую боль. Однако следует отметить, что указанное количество меньше рекомендуемого инструкцией.
Глубина достигаемой анестезии зависит не только от дозы, но и от времени экспозиции. Время экспозиции не должно быть менее 60 мин, а при обширных манипуляциях увеличивается как минимум вдвое. Сокращение времени аппликации допускается при нанесении препарата на слизистые оболочки, поврежденные кожные покровы и на участки с тонким эпидермисом (например, кожа вокруг глаз, губ) — в этом случае для обезболивания может быть достаточно даже 5–10 мин, но эффект длится в среднем 15–20 мин.
После 60-минутной аппликации под окклюзионной повязкой анестезия обеспечивается не менее чем на 2 мм в глубину кожи, а при увеличении времени экспозиции до 120 мин — не менее чем на 3 мм и продолжается около 2 ч [4].
Коррекции дозы для пожилых пациентов не требуется.
Препарат не конфликтует с вакцинами против кори, краснухи, эпидемического паротита, дифтерии, коклюша, столбняка, полиомиелита, гепатита В, а также гемофильной инфекции типа b. Однако из-за бактерицидного и противовирусного эффекта лидокаина и прилокаина в концентрациях 0,5–2% крем следует с особой осторожностью применять перед подкожным введением живой вакцины [4].
Побочные эффекты и меры предосторожности
Побочные нежелательные эффекты Анеста®-А, как и у его аналогов, в подавляющем большинстве случаев сопряжены с местными транзиторными реакциями на компоненты препарата в области его нанесения. Это может быть покраснение или побеление кожных покровов, отек, в некоторых случаях — легкое жжение, зуд и ощущение тепла. Эти явления обычно быстро проходят после удаления крема с кожи и не требуют лечения. При нанесении препарата на поврежденную кожу или язвы частота побочных реакций такого рода закономерно увеличивается.
Редко (< 0,1%) возможны аллергические реакции (в наиболее тяжелых случаях — вплоть до анафилактического шока), метгемоглобинемия.
Общетоксические реакции при соблюдении предписанных дозировок и рекомендаций по применению крайне маловероятны. Симптомы интоксикации такие же, как и при применении других местных анестетиков.
Применение Анеста®-А противопоказано [4]:
- если в анамнезе отмечалась повышенная чувствительность к анестетикам амидной группы или к любым другим компонентам препарата;
- у недоношенных новорожденных, родившихся при сроке беременности менее 37 нед;
- у новорожденных с массой тела менее 3 кг.
Препарат не наносят на открытые раны и в случаях, когда возможно его проникновение в среднее ухо (например, на поврежденную барабанную перепонку).
С осторожностью препарат следует использовать при недостаточности глюкозо-6-фосфатдегидрогеназы, наследственной или идиопатической метгемоглобинемии, на фоне назначения препаратов, вызывающих метгемоглобинемию, а также при приеме антиаритмических препаратов (токаинид, мексилетин и др.), в особенности III группы (амиодарон, соталол и др.).
При применении препарата на фоне распространенного нейродермита (атопического дерматита) необходимо учитывать, что для этого заболевания характерна более высокая проницаемость кожи, так что время экспозиции должно быть уменьшено до 15–30 мин.
Следует проявлять особую осторожность при нанесении крема на кожу в области глаз: при случайном попадании препарата в глаза возможно раздражение роговицы или ее повреждение. При случайном попадании крема в глаза их необходимо немедленно промыть водой или 0,9% раствором хлорида натрия, после чего закрыть пострадавший глаз до полного восстановления рефлексов.
При использовании Анеста®-А совместно с другими местными анестетиками и структурно сходными препаратами следует принимать во внимание риск усиления системных эффектов при использовании высоких доз. Кроме того, препараты, снижающие клиренс лидокаина (бета-адреноблокаторы, циметидин и др.), способны спровоцировать потенциально токсичные концентрации в плазме крови при применении повторных высоких доз лидокаина в течение продолжительного времени.
Хотя лидокаин и прилокаин способны проникать через плацентарный барьер и накапливаться в тканях плода, к настоящему времени нет достаточных данных, на основании которых можно было бы делать заявления об опасности применения препарата при беременности, равно как и не установлено его прямого или косвенного воздействия на репродуктивный процесс ни у животных, ни у человека. Нем не менее с целью снижения рисков препарат следует применять у беременных только при крайней необходимости, когда риск для матери превышает потенциальный риск для плода. Что касается грудного вскармливания, то экскреция лидокаина и прилокаина в грудное молоко при использовании препарата в терапевтических дозах не представляет риска для ребенка [4].
Применение продукции, в составе которой присутствуют незарегистрированные лекарственные вещества, может иметь негативные последствия для потребителей, так как в этом случае отсутствуют доказательная база и достоверные данные о безопасных дозировках, а также нет описания взаимодействия с другими лекарственными препаратами. Все это может привести к развитию токсических реакций, таких как головокружение, тошнота, тахикардия, а в тяжелых случаях — к летальному исходу. Использование зарегистрированных лекарственных средств дает возможность вести бизнес комфортно и безопасно!
Статья опубликована в журнале «Косметика и медицина» №3-2020
На правах рекламы
Литература:
- Матушевская Е.В., Свиршевская Е.В., Матушевская Ю.И., Коцарева О.Д. Топические местные анестетики в косметологии 2017; (3): 89–96.
- Lähteenmäki T., Lillieborg S., Ohlsén L., et al. Topical analgesia for the cutting of split-skin grafts: a multicenter comparison of two doses of a lidocaine/prilocaine cream. Plast Reconstr Surg 1988; 82(3): 458–
- You P., Yuan R., Chen C. Design and evaluation of lidocaine- and prilocaine-coloaded nanoparticulate drug delivery systems for topical anesthetic analgesic therapy: a comparison between solid lipid nanoparticles and nanostructured lipid carriers. Drug Des Devel Ther 2017; 11: 2743–
- Инструкция по медицинскому применению лекарственного препарата Анеста®-А. Регистрационный номер ЛП-005914-181119.
- Жигульцова Т.И., Паркаева Л.В., Ильина Е.Э., Виссарионов В.А. Опыт применения 5% крема «Эмла» в практике дерматокосметолога. Русский медицинский журнал 2008; 16(8): 570–571.
- Шарова А.А., Лебедюк В.Г. Анестезия в дерматокосметологии. Экспериментальная и клиническая дерматология 2010; (5): 36–41.
- Greveling K., Prens E.P., Ten Bosch N., van Doorn M.B. Comparison of lidocaine/tetracaine cream and lidocaine/prilocaine cream for local anaesthesia during laser treatment of acne keloidalis nuchae and tattoo removal: results of two randomized controlled trials. Br J Dermatol 2017; 176(1): 81–
- Horikiri M., Ueda K., Sakaba T. Comparison of Emla cream and topical lidocaine tape for pain relief of V-beam laser treatment. J Plast Surg Hand Surg 2018; 52(2): 94–
- Раннева Е.А. Применение крема Эмла в комплексной коррекции косметических недостатков. Экспериментальная клиническая дерматокосметология 2010; 2: 48–53.
- Lee S.H., Pakdeethai J., Toh M.P., Aw D.C. A Double-Blind, Randomised, Placebo-Controlled Trial of EMLA® Cream (Eutectic Lidocaine/Prilocaine Cream) for Analgesia Prior to Cryotherapy of Plantar Warts in Adults. Ann Acad Med Singap 2014; 43(10): 511–
- Mansell-Gregory M., Romanowski B. Randomised double blind trial of EMLA for the control of pain related to cryotherapy in the treatment of genital HPV lesions. Sex Transm Infect 1998; 74(4): 274–
- Hopkins C.S., Buckley C.J., Bush G.H. Pain-free injection in infants. Use of a lignocaine-prilocaine cream to prevent pain at intravenous induction of general anaesthesia in 1-5-year-old children. Anaesthesia 1988; 43(3): 198–201.


