ГЛУТАТИОН В ПРОГРАММАХ БОРЬБЫ С ПИГМЕНТАЦИЕЙ: МОЛЕКУЛЯРНО-КЛЕТОЧНЫЕ МЕХАНИЗМЫ И КЛИНИЧЕСКИЕ НАБЛЮДЕНИЯ
24.03.2026
Erid: 2RanyoJyarv
Ромашкина Анастасия Сергеевна
К.м.н., врач-дерматовенеролог, косметолог, трихолог, физиотерапевт,
врач превентивной медицины, член РОДВК, Общества детских дерматологов,
главный врач клиники дерматологии и косметологии Chistotel
Почему глутатион?
Цвет кожи, волос и глаз определяется количеством и типом меланина. Основная функция меланина — поглощение ультрафиолетовых (УФ) лучей и защита от их влияния. УФ‑излучение является ключевым внешним регулятором меланогенеза, повышая активность меланоцитов и через сигнальные пути усиливая экспрессию белков меланосом (включая ферменты меланогенеза, например тирозиназу), приводя в итоге к синтезу меланина.
Глутатион играет роль в процессах формирования пигмента по двум звеньям [1]. Во-первых, это редокс-баланс. Под действием УФ в коже образуются активные формы кислорода (АФК), участвующие в повреждении биомолекул и регуляции пигментации. При этом меланогенез является сам по себе кислородзависимым и сопровождается образованием АФК. В ряде моделей АФК рассматривают как сигнальные молекулы, способные стимулировать меланогенез. Таким образом, если уменьшить избыток АФК или изменить внутриклеточный редокс‑баланс, можно повлиять на интенсивность меланогенеза и проявления гиперпигментации.
Во-вторых, тиольные соединения в биохимии напрямую участвуют в меланогенезе. Восстановленный глутатион (GSH) и цистеин могут вступать в реакции с промежуточными продуктами пути на уровне «развилки» дофахинона [2]. Таким образом, глутатион влияет на пигментацию как через редокс‑среду клетки, так и через «химию» ранних стадий меланогенеза.
Меланогенез и «точки входа» глутатиона: базовая биохимия для клинического разговора
Основными цветовыми характеристиками кожи являются светлота и оттенок. Светлота показывает, насколько кожа выглядит светлой или темной, и определяется общим количеством меланина и особенностями его распределения.Оттенок описывает, «в какую сторону» смещен цвет (например, более коричнево‑черный или более красновато‑желтоватый), и может зависеть от соотношения эумеланина и феомеланина, хотя на него также влияют и другие хромофоры кожи.
Ключевой (и лимитирующий) фермент процесса — тирозиназа. Она катализирует начальные окислительные реакции, включая превращение L‑тирозина и/или L‑диоксифенилаланина (L-DOPA) в дофахинон. Этот этап традиционно рассматривается как основная «точка контроля» меланогенеза, поскольку без образования дофахинона дальнейшее построение полимерного пигмента невозможно (рис. 1).
Рис. 1. Пути меланогенеза [1]. Эумеланин и феомеланин производятся в результате многоступенчатого биохимического процесса, в котором фермент тирозиназа (TYR), ограничивающий скорость меланогенеза, использует L-тирозин и/или L-DOPA в качестве исходных субстратов. Сокращения: DHICA — DHI-2-карбоноваякислота; TRP-2 — дофахром-таутомераза.
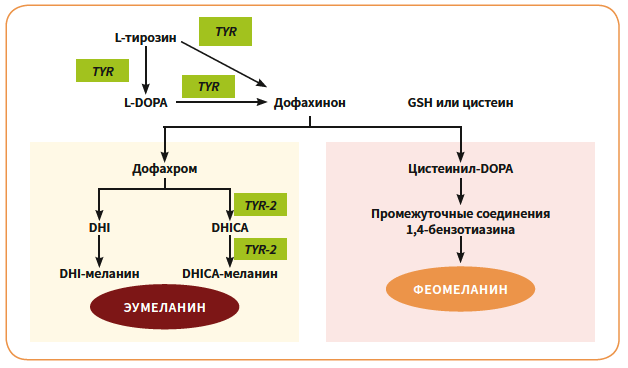
При обсуждении роли глутатиона важно учитывать «развилку» на уровне дофахинона [2].
- При достатке тиольных соединений (цистеина и GSH) дофахинон способен конъюгироваться с ними с образованием производных цистеинил‑DOPA и/или глутатионил‑DOPA. Далее эти соединения через бензотиазиновые промежуточные продукты окислительно полимеризуются, формируя серосодержащий пигмент — феомеланин [3, 4].
- При дефиците тиолов дофахинон идет по альтернативному пути: происходит внутримолекулярная циклизация с образованием дофахрома, затем — индольных производных, которые полимеризуются с формированием эумеланина.
В целом биохимия меланогенеза тесно связана с окислительно‑восстановительными реакциями.
Активность тирозиназы и последующие стадии синтеза меланина представляют собой последовательность окислительных превращений с высокой редокс‑активностью и, соответственно, повышенными требованиями к антиоксидантному контролю [2, 5].
АФК и пигментация: почему редокс‑баланс становится клинически значимым
УФ-излучение — ключевой внешний фактор, влияющий на пигментацию кожи. Один из центральных механизмов этого влияния связан с образованием АФК в коже, в числе которых — супероксидный анион (O2•−), пероксид водорода (H2O2) и гидроксильный радикал (OH•) [6, 7].
Оксидативный стресс сопровождает меланогенез и является одной из его биохимических составляющих. Меланогенез кислородзависим и включает последовательности окислительных реакций, которые сопровождаются образованием АФК. Например, при окислении L‑DOPA тирозиназой показано появление супероксида [8]. При окислительных превращениях ключевых предшественников эумеланина — DHI (5,6‑дигидроксииндол) и DHICA (5,6‑дигидроксииндол‑2‑карбоновая кислота) — сообщалось об образовании H2O2 как одного из сопутствующих продуктов этих реакций [9]. Иными словами, клетки, активно синтезирующие меланин, потенциально оказываются в условиях повышенной редокс‑нагрузки.
Редокс-нагрузка имеет клиническое значение: меланоцит должен одновременно синтезировать пигмент и защищаться от сопутствующего окислительного давления. В экспериментальных наблюдениях отмечали, что при усилении меланогенеза повышаются уровни АФК и снижается внутриклеточная концентрация GSH [10]. Таким образом, антиоксидантные системы обеспечивают устойчивость меланоцитов как к окислительной нагрузке, возникающей в ходе собственного метаболизма (включая меланогенез), так и к УФ‑индуцированным воздействиям.
АФК — не только повреждающие агенты, но и сигнальные молекулы, способные усиливать пигментацию. Показано, что низкие концентрации H2O2 (≤ 0,3 мМ) активируют тирозиназу и сопровождаются увеличением синтеза меланина в человеческих меланоцитах [11]. В других моделях H2O2 рассматривали как медиатор краткосрочной УФ-индуцированной меланогенной реакции [12]. Также описан УФ-А‑индуцированный ответ меланоцитов, где АФК выступают критическим внутриклеточным сигналом для продукции меланина во взаимодействии с кальциевой сигнализацией [13].
Резюмируя вышесказанное: «больше АФК» не всегда «только повреждение» — это сигнал к пигментообразованию. Если АФК способны поддерживать меланогенез в качестве сигнальных молекул, то их нейтрализация или смещение редокс‑потоков в сторону антиоксидантной защиты могут ослаблять стресс‑индуцированное усиление пигментообразования.
Антиоксидантная система кожи включает ферментные и неферментные звенья; в контексте данного обзора принципиально важно, что к ключевым неферментным антиоксидантам относится восстановленный глутатион (GSH), а изменения его доступности и соотношения восстановленной/окисленной форм могут иметь последствия для меланогенеза [14]. Это подводит к глутатиону как к компоненту антиоксидантной сети, который потенциально влияет на пигментацию как через редокс‑баланс, так и через прямое участие в «переключении» типа меланина — но эти два уровня действия важно разбирать отдельно и не смешивать в интерпретации [6].
Глутатионовая система: основа для понимания эффектов на пигментацию
Глутатион — один из наиболее распространенных внутриклеточных антиоксидантов [15]:
- В клетке есть запас глутатиона в двух формах: восстановленной (GSH) и окисленной (GSSG).
- Для нормальной работы клетки нужен достаточный запас глутатиона, а это возможно, только если система умеет быстро возвращать глутатион из окисленной формы обратно в восстановленную.
Синтез глутатиона идет в два шага (рис. 2). Сначала из L‑глутамата и цистеина образуется γ‑глутамилцистеин — эту реакцию катализирует глутамат‑цистеинлигаза (GCL). Затем глутатионсинтаза (GSS) присоединяет глицин, и образуется GSH. Для пигментации это важно: во многих ситуациях скорость синтеза глутатиона зависит от того, достаточно ли в клетке цистеина (в том числе поступающего в форме цистина). При этом тиолы — цистеин и сам глутатион — вовлечены и в меланогенез, влияя на реакции в точке развилки на уровне дофахинона [2, 16].
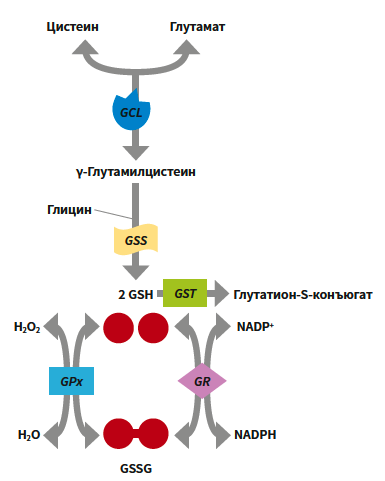 |
Рис. 2. Глутатионовая система |
Глутатионовая система — это не только молекула глутатиона. Это также ферменты, которые с ним «работают». Один из главных циклов связан с нейтрализацией пероксидов. Глутатионпероксидаза (GPx) использует GSH, чтобы превратить H2O2 в воду; в ходе реакции GSH окисляется и переходит в форму GSSG. Затем глутатионредуктаза (GR) восстанавливает GSSG обратно в GSH, используя NADPH как источник электронов [17]. С клинической точки зрения это означает следующее: способность меланоцита справляться с окислительной нагрузкой (как УФ‑индуцированной, так и связанной непосредственно с меланогенезом) зависит не только от количества внутриклеточного глутатиона, но и от того, насколько эффективно клетка умеет его регенерировать.
Кроме того, глутатион участвует в реакциях конъюгации с участием глутатион‑S‑трансферазы (GST), образуя глутатион‑S‑конъюгаты, то есть глутатион — донор тиольной группы в реакциях детоксикации и редокс‑регуляции; поэтому изменения его пула могут влиять на разные клеточные процессы, включая пигментообразование [18].
В практическом плане важно помнить, что глутатионовая система — это набор регулируемых звеньев: синтез глутатиона, обеспечение клетки цистеином/цистином и восстановление окисленного глутатиона [16, 17].
Как глутатион влияет на меланогенез: тирозиназа и «переключение» типа меланина
В обсуждении глутатиона как модулятора цвета кожи необходимо разграничить два разных, но взаимосвязанных механизма, а именно:
- Влияние на активность тирозиназы
- Влияние на направление потока меланогенеза в сторону эумеланина или феомеланина.
Оба механизма опираются на химическую природу глутатиона как тиольного соединения и его способность вступать в реакции с ключевыми промежуточными продуктами пути [2, 19].
Влияние глутатиона на тирозиназу: эффект зависит от концентрации
Экспериментальные данные показывают, что взаимодействие глутатиона с тирозиназой не сводится к простому ингибированию. Описан дозозависимый эффект: при концентрациях глутатиона ниже 3 мМ отмечали активацию тирозиназы, тогда как при более высоких концентрациях — ингибирование [19]. Практический смысл этой детали — в осторожности интерпретаций: «глутатион как осветляющий агент» не следует автоматически понимать как прямой блокатор тирозиназы в любых условиях. В реальной ткани и в разных экспериментальных моделях концентрации восстановленного глутатиона, его доступность в компартментах и скорость регенерации могут различаться, что теоретически способно смещать баланс эффекта.
С этим выводом согласуются наблюдения, что истощение глутатиона может сопровождаться усилением тирозиназной активности. В клеточной модели человеческой меланомы подавление синтеза глутатиона приводило к увеличению активности тирозиназы и «смещению» в сторону эумеланогенеза [20].
Переключение «эумеланин ↔ феомеланин»: GSH как тиольный перехватчик дофахинона
Второй механизм — более пигмент‑специфический. На уровне ключевого промежуточного метаболита — дофахинона — тиольные соединения способны менять дальнейшую судьбу продукта. Реакция тиольной группы GSH с дофахиноном приводит к образованию сульфгидрильного (тиольного) конъюгата; далее формируются серосодержащие промежуточные структуры и в итоге — феомеланин, а не эумеланин (см. рис. 1) [2, 19]. Получается, что глутатион — не просто антиоксидант, а компонент, который может участвовать в маршрутизации меланогенеза.
Важно подчеркнуть, что в обсуждениях осветления кожи этот механизм требует аккуратной клинической трактовки. Переключение в сторону феомеланина означает изменение типа пигмента, а не его общего количества. Это важно, чтобы правильно объяснить пациенту ожидаемые эффекты и их границы: вмешательство в редокс‑систему и тиольный статус может менять качественный состав меланина, а значит — не только оттенок кожи, но и то, как он ведет себя при воздействии УФ‑излучения (способность поглощать УФ и гасить фотоиндуцированные окислительные процессы) [2, 21].
С точки зрения стратегии терапии и ухода важно различать два возможных клинических исхода.
- Первый — снижение общей интенсивности меланогенеза: при воздействии на активность тирозиназы уменьшается скорость ранних стадий пути, снижается темп образования предшественников меланина и, как следствие, скорость накопления пигмента.
- Второй — изменение качественного состава пигмента: при «переключении» пути меняется соотношение эумеланина и феомеланина, и это может отражаться на характеристиках пигмента даже при сопоставимой исходной активности меланогенеза.
Регуляторы глутатионовой системы и меланогенез
При обсуждении влияния глутатиона на пигментацию возникает следующий вопрос: от чего зависит доступность GSH в меланоците? Отвечая на него, обычно выделяют три ключевых звена [22–24].
- Поставка цистина/цистеина. Транспортер xCT обеспечивает поступление цистина в клетку; далее он превращается в цистеин, который нужен для синтеза GSH. Поэтому xCT косвенно влияет на то, насколько устойчиво клетка обеспечена тиолами (цистеин/GSH), в том числе в точке развилки на уровне дофахинона [2, 23].
- Скорость синтеза GSH. GCL — фермент первого (лимитирующего) шага синтеза GSH [16]. Если это звено работает активнее, клетке проще наращивать пул GSH и поддерживать антиоксидантную защиту в условиях УФ‑индуцированной редокс‑нагрузки.
- Восстановление GSH из GSSG. GR восстанавливает GSSG до GSH и поддерживает восстановленный пул глутатиона. Для пигментации это важно, потому что доступность GSH влияет и на антиоксидантную устойчивость клетки, и на «тиольное давление» в реакциях меланогенеза [22].
Вместе xCT–GCL–GR определяют три практических параметра:
- насколько клетка может синтезировать GSH (фермент GCL);
- насколько эффективно она может поддерживать его в восстановленной форме (фермент GR);
- насколько стабильно она получает предшественники для синтеза (xCT → цистин/цистеин).
Это не готовые клинические мишени, а удобная схема для интерпретации экспериментальных данных. Если вмешательство усиливает антиоксидантный ответ и повышает доступность GSH, клетка лучше нейтрализует УФ‑индуцированные АФК и слабее запускает редокс‑зависимые сигналы, поддерживающие меланогенез [24, 25]. Кроме того, изменение доступности цистеина/GSH может влиять на реакции на уровне дофахинона, а значит — теоретически отражаться и на балансе типов меланина.
Клинические данные: пероральные, топические и парентеральные формы глутатиона для выравнивания тона кожи — что реально можно обещать врачу (и пациенту)
В клинических исследованиях эффект глутатиона на тон кожи оценивают по сочетанию объективных инструментальных методов (например, меланиновый индекс и показатели колориметрии/хромаметрии) и клинической/визуальной оценки.
Пероральный глутатион: эффект возможен, но это дополнение, а не замена базовой терапии
В систематическом обзоре Dilokthornsakul W. и соавт. (2019) отмечено, что пероральные и топические формы глутатиона в ряде исследований сопровождались положительными изменениями показателей, связанных с осветлением / улучшением параметров кожи, и в целом хорошо переносились. При этом число работ невелико, а дизайн и результаты исследований неоднородны, что ограничивает силу выводов. Важно также, что в этих работах не предлагается стандартизированного перечня противопоказаний для перорального глутатиона; данные по безопасности в основном представлены как описание нежелательных явлений. В частности, отмечались несерьезные события — преимущественно желудочно‑кишечные симптомы и кожные реакции (зуд/эритема/«красные пятна»), а также единичные случаи повышения печеночных ферментов с выбыванием участников; при этом часть кожных реакций фиксировалась и в группе плацебо [26].
В обзоре Sonthalia S. и соавт. (2018), посвященном глутатиону как средству для осветления кожи, авторы подчеркивают: у перорального пути есть определенная клиническая поддержка, но уровень доказательности недостаточен, чтобы обещать гарантированный и выраженный эффект у большинства пациентов [27].
Практический вывод:
- пероральный глутатион рациональнее обсуждать как дополнительный компонент программы выравнивания тона (на фоне фотозащиты и доказанных подходов к лечению гиперпигментации), особенно у пациентов со склонностью к реактивной пигментации после инсоляции или воспаления;
- если цель — быстрое и предсказуемое уменьшение пятен, это в первую очередь решается методами с более доказанным депигментирующим эффектом (топические депигментанты, лазерные процедуры, инъекционные препараты), а не только пероральным глутатионом [27].
Топические формы: самый мягкий вариант с точки зрения управляемости и переносимости
Топические формы привлекательны тем, что их легко интегрировать в ежедневный уход и в поддерживающую фазу после процедур. Наиболее аккуратно оформленные данные есть по топическому окисленному глутатиону (GSSG): в двойном слепом плацебо‑контролируемом исследовании у здоровых женщин показаны эффекты по параметрам, связанным с осветлением / улучшением состояния кожи [28]. С точки зрения безопасности в этом исследовании не регистрировали серьезных нежелательных явлений; отмечен единичный эпизод легкой эритемы на ранних сроках, который прошел без отмены средства [27]. В систематическом обзоре также подчеркнуто, что не было зарегистрировано нежелательных явлений для топического глутатиона, хотя вывод опирается фактически на очень ограниченную базу (одна небольшая работа по топическому GSSG) [26].
Практический вывод:
- топические формы — хороший выбор для пациентов, которым важны мягкость, переносимость и постепенность;
- в программах коррекции гиперпигментации их удобно использовать как поддержку результата, особенно когда врач хочет минимизировать раздражение от более активных депигментантов [27].
Парентеральный глутатион: клинических данных по людям мало, но биологическая база есть
Когда речь заходит о парентеральном введении (внутривенном или внутримышечном), важно сразу правильно расставить акценты: это не «сильнее, потому что укол», а другая степень медицинской ответственности. Парентеральный путь повышает требования к обоснованию назначения, мониторингу безопасности и к тому, как врач проговаривает ожидания и ограничения.
С позиции доказательной медицины картина остается осторожной: имеющиеся обзорные данные указывают, что клинических исследований на людях пока немного, они неоднородны по дизайну и исходам, поэтому выводы следует формулировать сдержанно. В разговоре с пациентом это лучше формулировать проще: имеющихся данных недостаточно, чтобы обещать гарантированный эффект [26, 27].
На этом фоне полезно понимать, что у темы есть биологическая поддержка на уровне доклинических моделей. В работе AlGhamdi K.M. и соавт. (2020) использовали коричневых морских свинок: гиперпигментацию у них индуцировали УФ-B‑облучением 3 раза в неделю на протяжении 3 нед, начиная с 250 или 500 мДж/см2 и затем постепенно повышая дозу до 1, 2, 4 и 6 Дж/см2; после подбора режима рабочей дозой для индукции гиперпигментации выбрали 6 Дж/см2. Далее животных оставляли на одну неделю без лечения для стабилизации изменений, после чего распределяли по четырем группам в зависимости от дозы глутатиона (контроль — физиологический раствор; 10, 20 или 40 мг/кг) и начинали введение препарата интраперитонеально 3 раза в неделю в течение 3 нед [29].
Эффект оценивали несколькими объективными уровнями: колориметрически по CIELAB (показатель светлоты L*), гистологически (окраска по методу Массон – Фонтана для визуализации меланина; рис. 3) и ультраструктурно (электронная микроскопия с оценкой меланосом и меланизированных клеток; рис. 4) [29]. В этой модели парентеральное введение глутатиона сопровождалось дозозависимым увеличением L* (то есть ростом светлоты кожи) и морфологическими признаками снижения меланизации на более высоких дозах. Для наглядности: в группе высокой дозы L* увеличивался примерно с 43,22 до 61,43. Параллельно авторы не выявили статистически значимых различий по стандартным лабораторным маркерам (AST/ALT, креатинин, BUN, общий анализ крови) и не обнаружили гистологических токсических изменений в печени, почках и легких в пределах длительности эксперимента.
Рис. 3. Гистологическое исследование, окрашивание по методу Массон – Фонтана, ув. ×600 [29]. А (контрольная группа) — в эпидермисе видна повышенная плотность меланиновых гранул (степень 3) в базальных меланоцитах (стрелка); распространение пигментации в некоторых областях до средних слоев эпидермиса. Б — фокальное и умеренное уменьшение плотности (до степени 1) меланиновых гранул в базальных меланоцитах (стрелка) после лечения глутатионом; оставшиеся гранулы занимают одну треть объема цитоплазмы.
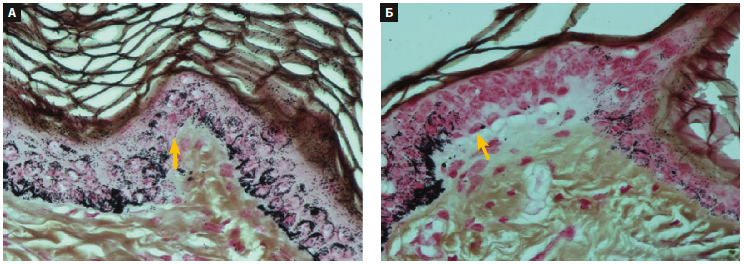
Рис. 4. Просвечивающая (трансмиссионная) электронная микроскопия: распределение зрелых меланосом (стадия IV) (стрелки) в надбазальных меланоцитах и кератиноцитах в коже различных экспериментальных групп животных. Ув. ×12 000 [29]. А — кожа контрольного животного: скопления зрелых меланосом; Б — кожа животного, обработанного 10 мг глутатиона/кг массы тела: почти нормальное распределение меланосом; В — кожа животного, обработанного 20 мг глутатиона/кг массы тела: меньше меланосом; Д — кожа животного, обработанного 40 мг глутатиона/кг массы тела: минимальное количество меланосом.
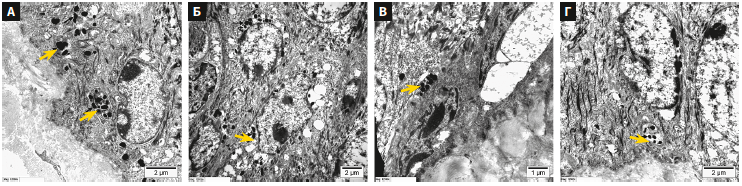
При этом принципиально важно проговорить ограничение: это животные и короткий срок наблюдения, поэтому работа помогает заложить фундамент под правдоподобность эффекта и краткосрочной переносимости в модели, но не заменяет клинических исследований у людей и не отвечает на вопрос долгосрочной безопасности [29].
Практический вывод: парентеральный глутатион уместно обсуждать только как потенциальный элемент комплексного подхода при приоритете базовых мер и аккуратной коммуникации ожиданий; доклинические данные объясняют, почему тема возникла, но не являются основанием для уверенных клинических обещаний [26, 27, 29].
Глатион в программах эстетической коррекции цвета кожи
Глатион — лекарственный препарат глутатиона. Он выпускается в форме лиофилизированного порошка для приготовления раствора для внутривенного и внутримышечного введения (РУ № ЛП-001337 (от 08.12.2011) и ЛП-№(005452)-(РГ-RU) (от 15.05.2024); производитель: Shandong Loui Pharmaceutical, Китай). Препарат выпускается во флаконах с содержанием действующего вещества 0,3; 0,6; 1,2 или 1,8 г; перед применением порошок разводят (как правило, стерильным 0,9% раствором хлорида натрия). Введение возможно внутривенно или внутримышечно; при внутривенном введении препарат вводят медленно, а конкретные дозировка и схема определяются врачом индивидуально.
С практической точки зрения важно, что у Глатиона есть понятная медицинская базовая роль: он используется как вспомогательное средство в комплексном лечении заболеваний печени у взрослых (включая острые и хронические гепатиты различной этиологии, алкогольный цирроз, стеатоз и фиброз печени). В дерматологии и эстетической медицине концепция применения другая: это не лечение кожи вместо дерматологической терапии, а поддерживающий инструмент для программ, где ключевыми патогенетическими звеньями выступают воспаление и оксидативный стресс — состояния, нередко сопутствующие фотоповреждению, постпроцедурным реакциям и поствоспалительным изменениям цвета кожи [30].
Клинически удобная рамка здесь простая: Глатион рассматривают не как средство «быстрого отбеливания», а как поддержку антиоксидантного фона и снижения реактивности кожи — чтобы она реже отвечала пигментацией на УФ, воспаление и раздражение [26, 27].
На практике это чаще всего обсуждается в понятных ситуациях:
- у пациентов с высоким риском гиперпигментации после воспаления или процедур — как поддержка в период уязвимости кожи при сохранении базовой терапии пятен и строгой фотозащиты;
- у реактивных пациентов при подготовке и реабилитации после пилингов/лазеров — как «фон» рядом с корректным постуходом и SPF;
- при фотостарении и неравномерном тоне на открытых участках — как дополнение, но не как основной депигментирующий инструмент;
- при хронических воспалительных дерматозах с поствоспалительными следами — только как поддерживающий компонент, не подменяющий стандартную терапию.
Пациенту необходимо донести следующую мысль: «Глутатион — не отбеливатель; основную работу делают фотозащита и базовые схемы. Здесь мы используем его как поддержку антиоксидантной защиты кожи: это может косвенно влиять на пигментацию и снижать склонность кожи отвечать усилением меланина на инсоляцию, воспаление или процедуры».
Важно заранее обозначать границы: не обещать гарантированного осветления и не позиционировать как замену терапии мелазмы. По парентеральным формам у людей доказательная база все еще ограниченна, а доклинические данные поддерживают биологическую правдоподобность, но не дают оснований для категоричных клинических обещаний [26, 27, 29].
Заключение
Глутатион в контексте коррекции цвета кожи стоит рассматривать не как отбеливающий агент, а как модификатор условий, в которых формируется и закрепляется гиперпигментация: оксидативного стресса, воспаления и общей реактивности кожи.
На уровне меланогенеза значимость глутатиона описывают как минимум в двух плоскостях — через редокс‑регуляцию и через влияние на направление пигментообразования в зоне «развилки» эу‑ и феомеланина. При этом клинические данные по осветлению кожи у людей существуют, но остаются ограниченными и неоднородными, поэтому глутатион корректнее позиционировать как компонент комплексной тактики, а не как самостоятельную терапию гиперпигментации.
Если говорить по формам, то для перорального пути чаще описывают умеренный «сигнал» улучшения параметров тона, особенно на открытых участках, но без гарантии выраженного эффекта у всех пациентов. Топические формы — прежде всего GSSG — выглядят наиболее «спокойным» вариантом для поддерживающей стратегии, хотя и здесь доказательная база ограничена числом исследований. Для парентеральных форм доказательная база у людей остается ограниченной; доклинические данные поддерживают биологическую правдоподобность и демонстрируют объективную динамику в модели, но не дают оснований для категоричных обещаний в эстетической практике.
Литература
- Lu Y., Tonissen K.F., Di Trapani G. Modulating skin colour: role of the thioredoxin and glutathione systems in regulating melanogenesis. Biosci Rep 2021; 41(5): BSR20210427.
- Ito S. High-performance liquid chromatography (HPLC) analysis of eumelanin and pheomelanin in melanogenesis control. J Invest Dermatol 1993; 100(2 Suppl): S166–S171.
- Napolitano A., Costantini C., Crescenzi O., et al. Characterization of 1,4-benzothiazine intermediates in the oxidative conversion of 5-S-cysteinyldopa to pheomelanins. Tetrahedron Lett 1994; 35: 6365–6368.
- Di Donato P., Napolitano A. 1,4-benzothiazines as key intermediates in the biosynthesis of red hair pigment pheomelanins. Pigment Cell Res 2003; 16(5): 532–539.
- Hearing V.J., Jimenez M. Mammalian tyrosinase: the critical regulatory control point in melanocyte pigmentation. Int J Biochem 1987; 19(12): 1141–1147.
- Nordberg J., Amer E.S. Reactive oxygen species, antioxidants, and the mammalian thioredoxin system. Free Radic Biol Med 2001; 31(11): 1287–1312.
- Liebel F., Kaur S., Ruvolo E., et al. Irradiation of skin with visible light induces reactive oxygen species and matrix-degrading enzymes. J Invest Dermatol 2012; 132(7): 1901–1907.
- Koga S., Nakano M., Tero-Kubota S. Generation of superoxide during the enzymatic action of tyrosinase. Arch Biochem Biophys 1992; 292(2): 570–575.
- Nappi A.J., Vass E. Hydrogen peroxide generation associated with the cooxidations of the eumelanin precursors 5,6-dihydroxyindole and 5,6-dihydroxyindole-2-carboxylic acid. Melanoma Res 1996; 6(5): 341–349.
- Smit N.P., van Nieuwpoort F.A., Marrot L., et al. Increased melanogenesis is a risk factor for oxidative DNA damage: study on cultured melanocytes and atypical nevus cells. Photochem Photobiol 2008; 84(3): 550–555.
- Tang L., Li J., Lin X., et al. Oxidation levels differentially impact melanocytes: low versus high concentration of hydrogen peroxide promotes melanin synthesis and melanosome transfer. Dermatology 2012; 224(2): 145–153.
- Tobin D., Thody A.J. The superoxide anion may mediate short- but not long-term effects of ultraviolet radiation on melanogenesis. Exp Dermatol 1994; 3(3): 99–105.
- Dumbuya H., Hafez S.Y., Oancea E. Ca2+ and ROS crosstalk regulate the UVA-induced melanin response in human melanocytes. FASEB J 2020; 34(9): 11605–11623.
- Ighodaro O.M., Akinloye O.A. First line defence antioxidants—superoxide dismutase (SOD), catalase (CAT) and glutathione peroxidase (GPx): their fundamental role in the entire antioxidant defence grid. Alex J Med 2018; 54(4): 287–293.
- Traverso N., Ricciarelli R., Nitti M., et al. Role of glutathione in cancer progression and chemoresistance. Oxid Med Cell Longev 2013; 2013: 972913.
- Lu S.C. Glutathione synthesis. Biochim Biophys Acta 2013; 1830(5): 3143–3153.
- Gallogly M.M., Starke D.W., Leonberg A.K., et al. Kinetic and mechanistic characterization and versatile catalytic properties of mammalian glutaredoxin 2: implications for intracellular roles. Biochemistry 2008; 47(42): 11144–11157.
- Gallogly M.M., Starke D.W., Mieyal J.J. Mechanistic and kinetic details of catalysis of thiol-disulfide exchange by glutaredoxins and potential mechanisms of regulation. Antioxid Redox Signal 2009; 11(5): 1059–1081.
- Jara J.R., Aroca P., Solano F., et al. The role of sulfhydryl compounds in mammalian melanogenesis: the effect of cysteine and glutathione upon tyrosinase and the intermediates of the pathway. Biochim Biophys Acta 1988; 967(2): 296–303.
- del Marmol V., Solano F., Sels A., et al. Glutathione depletion increases tyrosinase activity in human melanoma cells. J Invest Dermatol 1993; 101(6): 871–874.
- Thody A.J., Higgins E.M., Wakamatsu K., et al. Pheomelanin as well as eumelanin is present in human epidermis. J Invest Dermatol 1991; 97(2): 340–344.
- Benedetto J.P., Ortonne J.P., Voulot C., et al. Role of thiol compounds in mammalian melanin pigmentation. II. Glutathione and related enzymatic activities. J Invest Dermatol 1982; 79(6): 422–424.
- Chintala S., Li W., Lamoreux M.L., et al. Slc7a11 gene controls production of pheomelanin pigment and proliferation of cultured cells. Proc Natl Acad Sci U S A 2005; 102(31): 10964–10969.
- Panich U., Onkoksoong T., Limsaengurai S., et al. UVA-induced melanogenesis and modulation of glutathione redox system in different melanoma cell lines: the protective effect of gallic acid. J Photochem Photobiol B 2012; 108: 16–22.
- Chaiprasongsuk A., Onkoksoong T., Pluemsamran T., et al. Photoprotection by dietary phenolics against melanogenesis induced by UVA through Nrf2-dependent antioxidant responses. Redox Biol 2016; 8: 79–90.
- Dilokthornsakul W., Dhippayom T., Dilokthornsakul P. The clinical effect of glutathione on skin color and other related skin conditions: a systematic review. J Cosmet Dermatol 2019; 18(3): 728–737.
- Sonthalia S., Jha A.K., Lallas A., et al. Glutathione for skin lightening: a regnant myth or evidence-based verity? Dermatol Pract Concept 2018; 8(1): 15–21.
- Watanabe F., Hashizume E., Chan G.P., Kamimura A. Skin-whitening and skin-condition-improving effects of topical oxidized glutathione: a double-blind and placebo-controlled clinical trial in healthy women. Clin Cosmet Investig Dermatol 2014; 7: 267–274.
- AlGhamdi K.M., Kumar A., AL-Rikabi A.C., Mubarak M. Safety and efficacy of parenteral glutathione as a promising skin lightening agent: a controlled assessor blinded pharmacohistologic and ultrastructural study in an animal model. Dermatol Ther 2020; 33(2): e13211.
- Макаров Р.О. Глутатион в комплексных эстетических и дерматологических программах: эффективная поддержка здоровья и профилактика старения кожи. Косметика и медицина 2025; 1: 41–47.
Реклама. ООО "Фарпост"





