ПРОТОКОЛ ЛЕЧЕНИЯ ПАПУЛО-ПУСТУЛЕЗНОЙ ФОРМЫ РОЗАЦЕА С ПОМОЩЬЮ КОМБИНИРОВАННОГО ВОЗДЕЙСТВИЯ НЕОДИМОВЫМ ЛАЗЕРОМ 1064 НМ И КУРСОВОГО ПРИЕМА НИЗКОДОЗИРОВАННЫХ СИСТЕМНЫХ РЕТИНОИДОВ
14.10.2020
Евсюкова Зоя Александровна
Врач-дерматовенеролог, косметолог, челюстно-лицевой хирург, медицинский факультет Российского государственного социального университета, Университетская клиника Российского государственного социального университета, отделение дерматологии и косметологии, Москва.
Из существующих и широко распространенных методов лечения розацеа можно выделить два блока: симптоматическая и патогенетическая терапия. К симптоматической относится длительный (8-12 нед) прием антибиотиков тетрациклинового ряда (базисная терапия) [3–6], применение метронидазола и местных препаратов. Все эти методы лечения имеют широкий спектр побочных эффектов, включающих классические побочные эффекты от системной антибиотикотерапии: кандидоз, нарушения функций ЖКТ, а также специфичные для тетрациклинов — гиперпигментацию кожи и зубов, ввиду чего многие врачи во всем мире назначают макролиды (кларитромицин, эритромицин, джозамицин) [3, 7, 8]. Недостатком длительной антибиотикотерапии является и развитие штаммов бактерий, резистентных к препаратам тетрациклинового ряда и макролидам. Метронидазол назначают также длительно (4–8 нед) [9] на основании его противовоспалительного, а не акарицидного действия, как считалось ранее (роль Demodex Folliculorum в патогенезе розацеа считается слишком преувеличенной). Однако тяжелые соматические и вегетативные побочные эффекты от данного препарата, включающие головокружения, рвоту, зуд, антабусный эффект при одновременном приеме алкоголя даже в малых дозах, значительно ограничивают возможность назначения метронидазола.
Все большую популярность в лечении розацеа получают синтетические ретиноиды, назначаемые системно в дозах, значительно меньших, чем при терапии акне, однако на длительное время (до 6 мес) [12]. Влияние на процессы дифференцировки и кератинизации клеток сальных желез и эпидермиса делает ретиноиды незаменимыми в случае хронического воспалительного процесса сально-волосяных фолликулов при розацеа, однако ряд серьезных побочных эффектов, включающих тератогенное и гепатотоксическое действие, ограничивает возможности назначения препаратов этой группы.
Все большую популярность в лечении розацеа получают синтетические ретиноиды, назначаемые системно в низких дозах. Влияние на процессы дифференцировки и кератинизации клеток сальных желез и эпидермиса делает их незаменимыми в случае хронического воспалительного процесса сально-волосяных фолликулов при розацеа, однако ряд серьезных побочных эффектов, включающих тератогенное и гепатотоксическое действие, ограничивает возможности назначения препаратов этой группы.
Местная терапия розацеа применяется значительно шире, чем системная, что приводит к самолечению пациентов и формированию запущенных форм и стадий (фиматозных). По мнению Parodi A. et al. (2011) и Yentzer B.A. et al. (2010), монотерапия азелаиновой кислотой без применения пероральных антибиотиков ведет к хронизации процесса и отсутствию видимого эффекта [8, 15]. Метронидазол в виде 1% геля, применяемый наружно [3, 4, 7, 10], не одобрен FDA (the Food and Drug Administration), и в США его применение не санкционировано. Считается, что Demodex spp. выживают в условиях даже высоких концентраций метронидазола [11].
Местное использование синтетических ретиноидов исключает развитие характерных для них системных побочных явлений, однако также вызывает ретиноидный дерматит: сухость кожного покрова, шелушение, зуд [3–7, 11, 13]. Современные наружные средства используются в основном в виде кремов, содержащих метронидазол 0,75 и 1%, адапален 0,1%, азелаиновую кислоту, и гелей с метронидазолом 1% [1, 3, 4]. Наиболее оптимальным является комплексное применение азелаиновой кислоты, доксициклина (или клиндамицина) и метронидазола системно длительно [8, 11, 16].
В последние годы значительное распространение ввиду своей эффективности получил 1% крем пимекролимуса. Являясь производным макролактама аскомицина, он селективно ингибирует продукцию и высвобождение цитокинов и медиаторов из Т-лимфоцитов и тучных клеток. Доказано, что применение данного крема позволяет получить клиническую ремиссию у 82% больных [17, 18].
Традиционная местная терапия розацеа состоит из холодных примочек с антисептическими растворами (трихопол, 1–2% раствор борной кислоты, 1–2% раствор резорцина, отвар ромашки и т.д.), мазей, паст или кремов с противодемодекозным эффектом [1, 3].
Исходя из данных многочисленных исследований, наибольшую эффективность в лечении розацеа демонстрируют комбинированные медикаментозные и физиотерапевтические подходы.
Физиотерапевтическими методами, используемыми при розацеа, традиционно являются криотерапия, электрофорез, деструктивные методики.
Криотерапию проводят через день или ежедневно до глубокого отшелушивания. Метод показан больным независимо от стадии заболевания. Криотерапия оказывает противовоспалительное, сосудосуживающее, антипаразитарное действие [4, 7]. Клинические рекомендации также включают электрофорез с 10–30% раствором ихтиола 2–3 раза в неделю, с лидазой 2–3 раза в неделю, 10–15 сеансов [4]. Недостатком данных методов является их симптоматическая направленность, которая не удлиняет межрецидивный период, а также необходимость в частом посещении медучреждения, что для работающих, социально-активных пациентов является ограничивающим фактором.
В лечении папуло-пустулезной, кистозной и узловатой форм розацеа показаны деструктивные методики, такие как электрокоагуляция, дермабразия. Данные методы, к сожалению, имеют ряд недостатков: высокий риск послеоперационного инфицирования, лейкодермы, формирования эпидермальных кист и рубцов [3, 4, 7] и постепенно теряют свою актуальность не только в связи с имеющимися побочными эффектами, но и по причине низкой эффективности по сравнению с лазерным облучением [19] — методом, обеспечивающим наиболее эффективный и продолжительный результат лечения розацеа [2–5, 7, 11, 19, 20].
В зависимости от энергетических характеристик лазера выделяют низкоэнергетические с плотностью мощности менее 100 мВт/см2 и высокоэнергетические лазеры с плотностью мощности более 10 Вт/см2. От мощности лазера напрямую зависят фотобиологические эффекты, которые он вызывает. Низкоинтенсивное лазерное излучение (НИЛИ) сопряжено с фотохимическими реакциями. Фототермические эффекты высокоинтенсивного лазерного излучения (ВИЛИ) вызывают локальную деструкцию посредством фотодинамического действия, фотокоагуляции или фотоабляции [2].
Избирательное фототермическое или фотоакустическое действие ВИЛИ объясняется теорией селективного фототермолиза (СФТ), согласно которой для повреждения или разрушения целевого хромофора необходимо, чтобы коэффициент поглощения энергии лазерного излучения мишенью и окружающей тканью максимально различались, а длительность импульса была меньше или равна времени термической релаксации [2].
Открытие СФТ сделало возможным воздействие на специфические хромофоры кожи без повреждения окружающих структур путем подбора соответствующей длины волны, длительности импульса и плотности энергии. То есть параметры лазерного излучения могут быть оптимизированы таким образом, чтобы точно воздействовать на ткань-мишень с минимальным сопутствующим повреждением других тканей.
Хромофором, на который направлено воздействие при лечении сосудистых образований, является оксигемоглобин [19]. Наибольшее поглощение излучения оксигемоглобином происходит при длине волны 542, 577 нм. В результате поглощения оксигемоглобином лазерного излучения сосуд подвергается воздействию энергии и коагулируется [19].
Для лечения сосудистой патологии кожи применялись с той или иной степенью эффективности и безопасности различные виды лазеров. Первым большим достижением лазерной терапии сосудистых образований было создание в 1970 г. аргонового лазера с длиной волны 488 и 514 нм. К сожалению, использование лазерной установки, генерирующей непрерывное излучение, вызывало коагуляционный некроз поверхностных слоев кожи, что часто вело к последующему образованию рубцов и депигментации [19].
Параметры лазерного излучения могут быть оптимизированы таким образом, чтобы точно воздействовать на ткань-мишень с минимальным сопутствующим повреждением других тканей. При розацеа улучшение очищения кожи лица от телеангиэктазий и уменьшение выраженности эритемы могут быть достигнуты наложением импульсов с меньшей плотностью светового потока, но с большей длительностью, что позволяет также избежать появления пурпуры после лечения.
Улучшение очищения кожи лица от телеангиэктазий и уменьшение выраженности эритемы могут быть достигнуты наложением импульсов с меньшей плотностью светового потока, но с большей длительностью, что позволяет также избежать появления пурпуры после лечения. По данным Голдберга Дж. (2010), степень очищения кожи после одного сеанса лечения увеличилась с 67% при использовании неперекрывающихся импульсов до 87% после применения методики наложения импульсов [19]. Осложнения после применения импульсного лазера на красителе (pulsed dye laser, PDL), такие как гиперпигментация, атрофия, гипертрофический рубец, экзематозный дерматит, встречаются крайне редко [19]. Последние исследования доказали терапевтическую результативность ВИЛИ с длиной волны 578 нм, которая составляет при эритематозно-телеангиэктатической форме 88%, при папулезной — 83,7%, при пустулезной — 76,3%, при инфильтративно-пролиферативной — 62,7%. Отдаленные результаты данного исследования показали, что спустя три года достигнутый эффект в среднем сохраняется у 21% пациентов [22].
Отмечено, что при преобладании в клинической картине телеангиэктазий показан метод лазерной бесконтактной коагуляции с помощью диодного или неодимового лазера [2, 23]. По мнению некоторых авторов, в лечении розацеа также эффективны генераторы интенсивного импульсного света (intense pulsed light, IPL) c длиной волны 500–1200 нм и максимумом эмиссии в диапазоне 530–700 нм. При поверхностных телеангиэктазиях диаметром до 0,3 см действенный эффект отмечен при длине волны 530–600 нм (желто-зеленый спектр) [2, 21]. Имея широкий диапазон длины волны, излучение способно достигать сосудов-мишеней, расположенных на различной глубине от поверхности кожи.
Несмотря на то, что излучение с большой длиной волны проникает глубже, уровень поглощения энергии оксигемоглобином уменьшается. Поэтому для компенсации снижения абсорбции энергии требуется увеличение плотности потока излучения, что и применяется в данном типе устройств. Таким образом, эффективно нагреваются как поверхностные, так и глубокорасположенные сосуды, размер пятна, образуемого излучением, также достаточно велик. Другим вероятным преимуществом IPL является то, что энергия лазерного излучения доставляется к ткани-мишени с помощью импульса большей длительности. Это ведет к более равномерному нагреванию, коагуляции всего патологически измененного сосуда [19, 21, 23]. Лазеры на парах тяжелых металлов имеют ограничения в применении, так как в данном случае энергия лазерного излучения поглощается не только оксигемоглобином, но и меланином, содержащимся в эпидермисе и дерме. Поэтому такие лазеры применяются для лечения пациентов только со светлой кожей (тип I и II по Фицпатрику). У пациентов с темной кожей высок риск нарушений пигментации, появляющихся вслед за воспалительной реакцией, как правило, это образование пузырей и струпа [19, 23].
В случае преобладания в клинической картине телеангиэктазий показан метод лазерной бесконтактной коагуляции с помощью диодного или неодимового лазера [2, 23]. Nd:YAG-лазер (1064 нм) позволяет проникнуть в дерму и коагулировать кровеносных сосудов на глубине 2–3 мм от дермоэпидермального соединения. Диодные лазеры (800, 810, 930 нм) генерируют излучение с большей длиной волны, которое соответствует области минимального поглощения гемоглобином, что делает их теоретически более подходящими для лечения крупных глубокорасположенных сосудов диаметром 0,4 мм [19].
Другие системы, использующиеся для лечения сосудистых образований, — это калий-титанил- фосфатный (КТФ) лазер, длинноимпульсный лазер на алюмоиттриевом гранате с неодимом (Nd:YAG), длинноимпульсные лазеры на александрите (755 нм) и диодные лазеры (800, 810, 930 нм). КТФ-лазер — это Nd:YAG-лазер с удвоением частоты, генерирующий излучение в диапазоне 532 нм (зеленый свет). Длина волны 532 нм приближается к одному из пиков поглощения излучения гемоглобином, поэтому хорошо подходит для коррекции поверхностных кровеносных сосудов [19, 21]. На длине волны 1064 нм Nd:YAG-лазер позволяет проникнуть в дерму намного глубже. При этом может быть достигнута коагуляция кровеносных сосудов на глубине 2–3 мм от дермоэпидермального соединения. Это позволяет иметь в качестве цели более глубокую сосудистую сеть, которую PDL может быть не в состоянии достигнуть. Эти глубокие крупные кровеносные сосуды обычно требуют продолжительности импульса между 3 и 15 мс. Так как абсолютное поглощение гемоглобином энергии лазерного излучения при длине волны 1064 нм ниже, чем при длине волны 585 нм, с этой длиной волны должна использоваться значительно более высокая плотность потока. Вследствие этого для данного лазера охлаждение стоит на первом месте [20, 23].
Длинноимпульсные лазеры на александрите (755 нм) и диодные лазеры (800, 810, 930 нм) генерируют излучение с большей длиной волны, которое соответствует области минимального поглощения гемоглобином, что делает их теоретически более подходящими для лечения крупных глубокорасположенных сосудов диаметром 0,4 мм [19].
По мнению Голдберга Дж. (2010), в лазерной терапии розацеа определенные трудности представляют сосудистые образования крыльев носа. Для удаления телеангиэктазий в этой области необходимо многократное проведение лечебных сеансов и, возможно, повторного курса лечения в будущем [19]. Эритема лица поддается лечению одинаково хорошо как с использованием PDL, так и c IPL [10, 20].
Современная терапия стоит на пороге лечения дерматозов комбинированием различных методов. Оптимизировать клинический результат и уменьшить риск побочных эффектов возможно при сочетанном применении фракционного неселективного лазера и IPL; углекислотного (СО2) лазера и радиочастотной (radiofrequency, RF) технологии, лазера и фотодинамической терапии (ФДТ) [24, 25].
Современная терапия стоит на пороге лечения дерматозов комбинированием различных методов. Оптимизировать клинический результат и уменьшить риск побочных эффектов возможно при сочетанном применении фракционного неселективного лазера и IPL; углекислотного (СО2) лазера и радиочастотной (radiofrequency, RF) технологии, лазера и фотодинамической терапии (ФДТ) [24, 25].
На сегодняшний день одним из самых дискутируемых вопросов является применение лазерной ФДТ. Терапевтическое действие ФДТ основывается на фотохимических реакциях, происходящих при взаимодействии порфиринов, лазерного излучения и кислорода. В данном случае лазер является активатором фотохимических процессов в клетках и не вызывает фототермического повреждения. Для ФДТ может применяться любой лазер с длиной волны 400–800 нм [2]. Однако данный метод тоже не лишен недостатков. Побочные эффекты проявляются фототоксическими реакциями в виде эритемы, отека, корочек, эрозий, везикул, что, как правило, наблюдается у большинства пациентов и носит преходящий характер, а также возможного возникновения гиперпигментаций на месте проведения ФДТ [2].
При инфильтративно-продуктивной стадии розацеа показаны деструктивные методы, поскольку имеющиеся ультраструктурные изменения в системе микроциркуляторного русла кожи лица носят необратимый характер. В этом случае применяют лазерную абляцию с целью удаления гипертрофированной «фиматозной» ткани [5], которую проводят до достижения уровня сальных желез. При этом возможно использование импульсного СО2-лазера или фракционного эрбиевого (Er:YAG) лазера с модулированным импульсным режимом [2]. Применение данных типов лазеров является «золотым стандартом» аблятивных процедур, альтернативных традиционному хирургическому подходу к этой проблеме [5, 7].
Однако при лечении СО2- или Er:YAG-лазером наблюдается длительное заживление раневого дефекта и повышается риск развития таких явлений, как замедленная реэпителизация, стойкая эритема, гипопигментация кожи, а в некоторых случаях — формирование гипертрофических и келоидных рубцов.
При всех формах розацеа показаны курсы низкоэнергетического лазерного воздействия, которое проводят через день (6 процедур), среднее время воздействия составляет 25 мин [2].
Буквально недавно (в июне 2020 г.) в США вышла статья [26], опубликованная в Journal of Drugs in Dermatology, в которой авторы (Голд М., Мантурова Н., Круглова Л.) описывают результаты сочетанного метода терапии акне легкой и средней степени тяжести с помощью короткоимпульсного неодимового лазера на иттрий-алюминиевом гранате с длиной волны 1064 нм и длительностью импульса 0,65 мс (650 мкс) в комбинации с низкими дозами системного изотретиноина (0,2–0,3 мг/кг/сут) у пациентов, имеющих атрофические рубцы, а также выявленный полиморфизм генов ММР1, ММР3, ММР7, Col1A2, ESR7, что, по их мнению, может приводить к появлению рубцов. Всем пациентам проводилось 12 сеансов лазерного лечения с 2-недельными интервалами. Результатами данного 6-месячного исследования стало не только клиническое выздоровление от акне, но и уменьшение выраженности атрофических рубцов, что позволило авторам сделать заключение о безопасности сочетания неаблятивного лазерного воздействия короткоимпульсным лазером (в исследовании применялся Aerolase light Pod Neo) с низкодозированными синтетическими системными ретиноидами, а также о положительном влиянии на синтез коллагена, приведшем к уменьшению выраженности атрофических рубцов.
Таким образом, несмотря на некоторые ограничения, лазеры и устройства с источниками света остаются наилучшим выбором в лечении сосудистых поражений кожи [10, 20].
В течение последних 5 лет в мировой практике лечения розацеа на первом плане представлены именно лазерные технологии и технологии IPL. Авторы расходятся во мнениях, какой метод более безопасный, в первую очередь поскольку эффективность обоих методов достаточно высока и позволяет избегать классических медикаментозных методов лечения с их обширным перечнем системных побочных эффектов и более низким клиническим результатом.
Материалы и методы
Для выявления наиболее эффективного, быстрого и безопасного метода лечения розацеа нами были отобраны две относительно однородные по численности, полу, весовой категории и возрасту группы пациентов.
Одна группа пациентов прошла курс терапии с помощью неодимового лазера Nd:Yag 1064 нм Aerolase Neo. В свою очередь, вторая группа пациентов получала комбинированную терапию, включающую прием системных ретиноидов в суточной дозе 8 мг (препарат изотретиноин компании «Ядран», Хорватия) и периодическое воздействие лазером Nd:Yag 1064 нм Aerolase Neo. Все пациенты получали уход за кожей по показаниям в зависимости от качеств и состояния рогового слоя эпидермиса, увлажненности и чувствительности кожи. Среди уходовых средств был успокаивающий крем Bioderma Cicabio, который назначался всем пациентам как средство восстановления после лазерного воздействия в первые 3 дня после процедуры; с 4-го дня все пациенты использовали увлажняющий крем для чувствительной кожи Bioderma Sensibio Rich или Bioderma Sensibio Light с частотой 2 раза в день, согласно рекомендациям.
Очищение кожи проводилось мицеллярной водой Bioderma, кратность очищения кожи варьировала от 2 до 5 раз в день — по мере индивидуальной необходимости. Результаты лечения оценивались ежемесячно, фотопротоколировались, а также оценивались пациентами в начале и в конце лечения с помощью опросника на определение индекса качества жизни.
Исследование проводилось в период с августа 2019 по март 2020 года на базе Медицинского факультета Университетской клиники РГСУ (Москва). В исследовании приняли участие 38 пациентов (по 19 в каждой группе), средний возраст пациентов составил 38 лет, все пациенты имели I и II фототипы кожи по Фицпатрику, а также близкие значения ИМТ (средняя масса тела составила 56 кг).
Результаты
В ходе проведенного нами исследования обнаружено, что положительные результаты лечения достигнуты в обеих группах, причем скорость наступления регресса была одинаково быстрой: уже после первой процедуры лазерного воздействия количество высыпаний уменьшилось до 50%, а морфологические элементы сыпи регрессировали в инволюционном порядке: инфильтраты размягчались, пустулы «подсыхали», папулы уменьшались в размере и полностью исчезали, а общая яркость и морфологическое разнообразие клинической картины стихали. Скорость же полного выздоровления была более быстрой во второй группе, в которой пациенты получали минимальную суточную дозу системных ретиноидов (из расчета 0,14 мг/кг/сут), что позволило сократить курс лазерного лечения на 2 процедуры. При этом ретиноиды отменялись при полном клиническом выздоровлении, без необходимости набора курсовой кумулятивной дозы, как в случае лечения обыкновенных угрей. Динамика клинической картины в группе комбинированной терапии представлена на рис. 1–4.
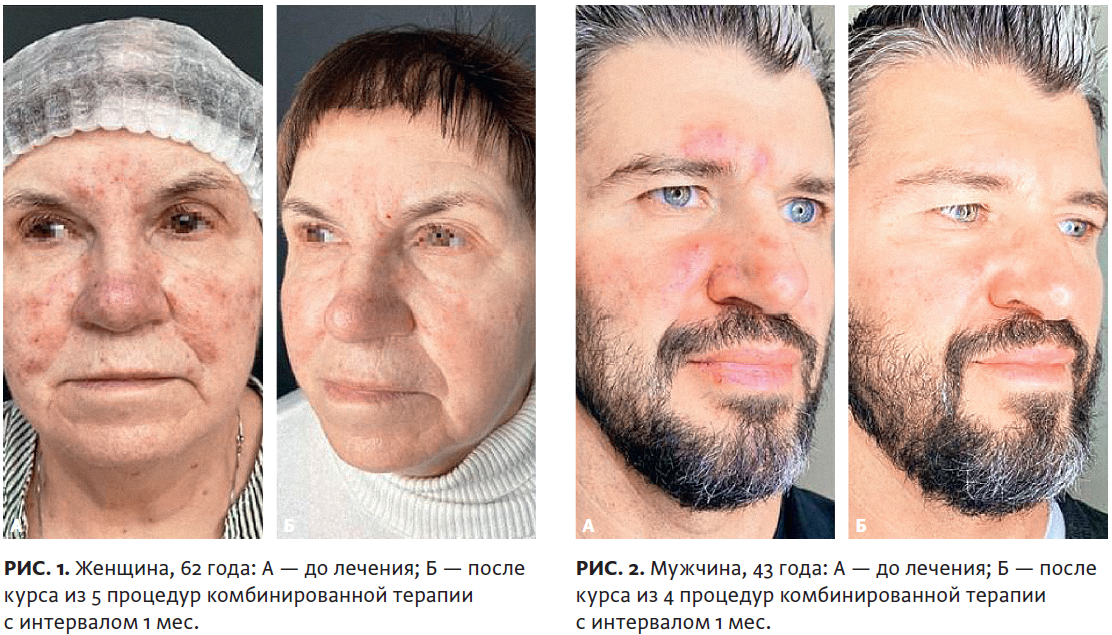
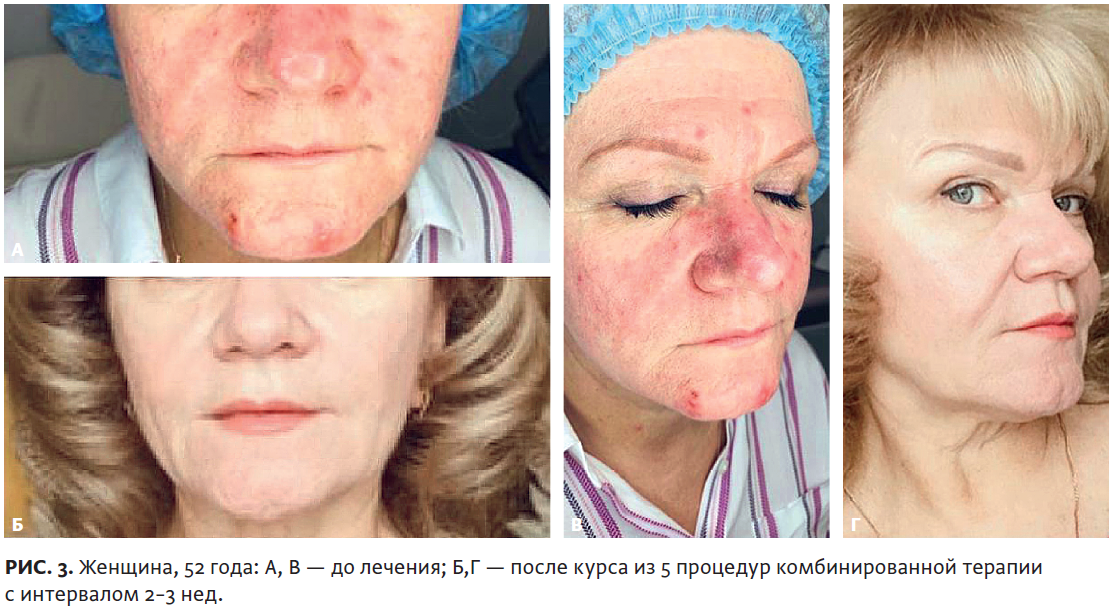
Следует также отметить, что в первой группе, получавшей только лазерное лечение, ввиду наличия 2 дополнительных процедур лазерного воздействия, наблюдался омолаживающий эффект в виде повышения тонуса и качества кожи, уменьшения борозд и складок, являющихся проекцией септ, разделяющих жировые компартменты гиподермы, что объясняется результатом термостимуляции коллагеновых структур и лимфооттока. Интересно, что часть пациентов обеих групп на том или ином этапе терапии подвергались инсоляции (на горнолыжных курортах или морских побережьях) с применением фотозащитных средств Bioderma Photoderm AR SPF 50+, что ранее считалось опасным с точки зрения риска фотоповреждения на фоне приема системных ретиноидов и лазерной терапии, однако ни у одного пациента не возникло подобных нежелательных явлений.
Обсуждение
Исходя из обзора существующих на сегодняшний день методов лечения розацеа, можно выделить наиболее эффективные, патогенетически обоснованные методы, такие как терапия широкополосным светом (IPL), фотодинамическая терапия и терапия неодимовыми лазерами, среди которых стоит выделить лазер Aerolase light Pod Neo с длиной волны 1064 нм и короткой длительностью импульса (0,6 мс), что меньше времени термической релаксации сосуда, который видится нами вариантом предпочтения как наиболее безопасный при наличии всех существующих рисков (внешние и внутренние фотосенсибилизирующие факторы, риск нецелевого прогрева окружающих тканей с вероятностью последующих термических ожогов структур дермы) и при этом максимально эффективный ввиду высокой мощности и проникающей способности неодимового лазера.
Предложение метода
Метод лазерного лечения с помощью аппарата Aerolase light Pod Neo как патогенетически обоснованный и достаточно эффективный может рекомендоваться для терапии розацеа в качестве самостоятельного метода, а также в комбинации с низкодозированной системной терапией ретиноидами.
Преимущества данного метода очевидны и весомы: быстрое наступление клинического улучшения по сравнению с «классическими» способами лечения розацеа, экономическая целесообразность (процедуры выполняются с частотой 1 раз в месяц при курсе 4–6 процедур), отсутствие побочных эффектов, легкая переносимость терапии, а также стойкость полученного результата.
Немаловажным фактором является «побочный» эффект в виде сглаживания борозд, укрепления овала лица, улучшения тонуса и упругости кожи, что значительно повышает комплаентность пациентов при выбранном методе лечения, а также их качество жизни.
Заключение
Данная методика может быть рекомендована для широкого клинического применения ввиду ее эффективности, относительной экономичности и безопасности. Необходимость дополнительного назначения низкодозированных синтетических системных ретиноидов решается врачом индивидуально для каждого пациента в зависимости от показаний (большое количество кистозных и инфильтративных элементов) и противопоказаний, которые зачастую являются весомыми факторами для выбора метода лазерной монотерапии.
Статья опубликована в журнале «Аппаратная косметология» №3/2020
На правах рекламы
Литература
- Волкова Е.Н., Осипова Н.К., Родина Ю.А., Григорьева А.А. Розацеа: новые подходы к старым проблемам. Российский журнал кожных и венерических болезней. 2010; 2: 33–39.
- Потекаев Н.Н., Круглова Л.С. Лазер в дерматологии и косметологии. М.: МВД, 280 с.
- Потекаев Н.Н. Розацеа. М.-СПб: ЗАЩ «Издательство БИНОМ»; «Невский диалект», 2000. 144 с.
- Клинические рекомендации. Дерматовенерология / под ред. А.А. Кубановой. М.: ДЭКС- Пресс, 2007. 300 с.
- Европейское руководство по лечению дерматологических заболеваний / под ред. А.Д. Кацамбаса, Т.М. Лотти. М.: МЕДпресс-информ, 2008. 736 с.
- Kanada K.N., Nakatsuji , Gallo R.L. Doxycycline indirectly inhibits proteolytic activation of tryptic kallikrein-related peptidases and activation of cathelicidin. J Invest Dermatol 2012; 132(5): 1435–1442.
- Адаскевич В.П. Актуальная дерматология. Н.-Новгород: Изд-во НГМА, 2000. 306 с.
- Parodi , Drago F., Paolino S., et al. Treatment of rosacea. Ann Dermatol Venereol 2011; 138(Suppl 3): S211–214.
- Djukic K. Recidivans Rosacea papulo pustulosa due to recidivans pylori. 9 th EADV Spring Symposium, Verona, Italy, 2012, p. 183.
- Kennedy Carney C., Cantrell , Elewski B. E. Rosacea: a review of current topical, systemic and light-based therapies. G Ital Dermatol Venereol 2009; 144(6): 673–688.
- Руководство по дерматокосметологии / под ред. Е.Р. Аравийской и Е.В. Соколовского. СПб: ООО «Издательство Фолиант», 2008. 632 с.
- Aksoy , Altaykan-Hapa A., Egemen D., et al. The impact of rosacea on quality of life: effects of demographic and clinical characteristics and various treatment modalities. Br J Dermatol 2010; 163(4): 719–725.
- Nevoralova Z. A patient with steroid-induced rosacea, colitis ulcerosa and polymyositis successfully treated by peroral isotretinoin- a case report. 9 th EADV Spring Symposium, Verona, Italy, p. 179.
- Перламутров Ю.Н., Сайдалиева В.Ш., Ольховская К.Б. Сравнительная оценка эффективности различных методов терапии розацеа. Вестник дерматологии и венерологии 2011; 3: 73–79.
- Yentzer A., Fleischer A.B. Changes in rosacea comorbidities and treatment utilization over time. J Drugs Dermatol 2010; 9(11): 1402–1406.
- Zuuren E.J., Kramer S., Carter B., et al. Interventions for rosacea. Cochrane Database Syst Rev 2011; (3): CD003262.
- Додина М. И. Клинические, иммунологические и морфологические взаимосвязи у больных розацеа на фоне лечения пимекроклимусом. Автореф. дис. … канд. мед. наук. М., 2011. 25 с.
- Sparavigna A., Palmieri R., Caserini M. Derming S.R.l. Activity of P-3075, a new medical device based on potassium azeloyl diglycinate, on the microcirculation in patients with rosacea. 9 th EADV Spring Symposium, Verona, Italy, p. 82.
- Голдберг Дж. Д Лазеро- и светолечение. Т. М.: ООО «Рид Элсивер», 2010. 187 с.
- Goldberg D.J. Lasers and light sources for rosacea. Cutis 2005; 75(3 Suppl): 22–26; discussion 33–36.
- Dahan S. Laser and intense pulsed light management of couperose and rosacea. Ann Dermatol Venereol 2011; 138(Suppl 3): S219–222.
- Дубровина А.А. Коррекция гемодинамических нарушений при розацеа высокоинтенсивным лазерным излучением. Автореф. дис. … канд. мед. наук. СПб., 2011. 20 с.
- Bernstein E. The pulsed-dye laser for treatment of cutaneous conditions. G Ital Dermatol Venereol 2009; 144(5): 557–572.
- Bjerring Present and future trends of vascular and pigmented lasers. 9 th EADV Spring Symposium, Verona, Italy, 2012. p. 157.
- Leonardo L. Combination treatments in laser dermatology. 9 th EADV Spring Symposium, Verona, Italy, p. 12
- Gold M.H., Manturova N., Kruglova L., Ikonnikova E.V. Treatment of Moderate to Severe Acne and Scars With a 650-Microsecond 1064-nm Laser and Isotretinoin. J Drugs Dermatol 2020; 19(6): 646–651.